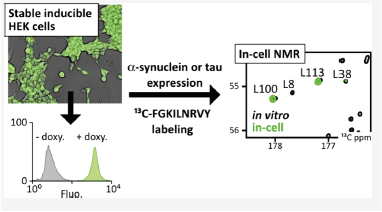
Les agrégats de protéines non globulaires sont associés à plusieurs troubles dégénératifs, par exemple l'α-synucléine et la protéine tau impliquées dans les maladies de Parkinson et d'Alzheimer. Ces protéines subissent-elles des changements progressifs dans leurs conformations et leurs interactions dans des situations pathologiques ? La RMN intracellulaire fournit des informations à l'échelle atomique dans des cellules vivantes, mais jusqu'à présent, uniquement à environ 283 K dans le cas des protéines dépliées. Nous présentons ici de nouvelles méthodes de marquage et d'acquisition permettant la RMN intracellulaire à 310 K afin d'étudier ces protéines à des concentrations micromolaires, c'est-à-dire à des abondances cellulaires natives. Nous avons utilisé des lignées cellulaires humaines stables exprimant l'α-synucléine ou la protéine tau après induction dans un milieu de culture supplémenté en acides aminés marqués au 13C ou en précurseurs de ceux-ci. L'acquisition de spectres 13Cα-13CO a permis une analyse précoce résolue par résidu de l'α-synucléine et de la protéine tau à 310 K et <10μM dans des cellules HEK à 700 MHz. Nous avons détecté des conformations désordonnées et des schémas d'interactions cellulaires étendues pour l'α-synucléine de type sauvage et deux mutants (F4A, A30P), ce qui suggère l'apparition d'une sous-population se liant à la membrane lipidique à 310 K. Seule l'extrémité N-terminale désordonnée de la protéine tau était observable, même après démantèlement des microtubules par la colchicine. Cela montre que des partenaires de liaison supplémentaires interfèrent avec la protéine tau dans les cellules. Notre approche offre une excellente évolutivité, en termes de signal et de résolution, jusqu'à 1,2 GHz. Le marquage 13C et la spectroscopie RMN détectée par 13C dans des cellules humaines vivantes sont donc des techniques viables pour la biologie structurale intracellulaire.
Article : https://pubs.acs.org/doi/full/10.1021/jacs.5c15061